Europejska Komisja Leków (EMA) zatwierdziła »szczepienie Covid« dla niemowląt od 6. miesiąca życia. Oznacza to, że spadł również ostatni próg zahamowania w odniesieniu do grup wiekowych. To ponownie wywołało pytania o niezależność EMA w podejmowaniu decyzji dotyczących zezwolenia.
Jak naprawdę niezależna jest EMA?
Niespodzianka finansowania EMA
Wielu obywateli zakłada, że EMA jest agencją UE i jest przez nią w pełni finansowana. Ale daleko od tego – to nie odpowiada faktom:
Według aktualnego budżetu rocznego Europejskiej Agencji Leków EMA na 2022 r., 86% pochodzi bezpośrednio z opłat i należności przemysłu farmaceutycznego.
Tylko 13% pochodzi z UE. Tylko 1% pochodzi z innych źródeł. EMA jest zatem w dużej mierze finansowana przez firmy farmaceutyczne. Wbrew ogólnej idei niezależnego organu ds. leków prowadzonego przez UE, EMA okazuje się znacznie bardziej uzależniona od wpłat i honorariów firm farmaceutycznych.
Pytanie brzmi, co w rezultacie z niezależnością w obszarze kontroli bezpieczeństwa leków i szczepionek?
I nie tylko finansowanie rodzi pytania: Emer Cooke, były długoletni przedstawiciel przemysłu farmaceutycznego, awansował na szczyt EMA właśnie w czasie kampanii szczepień przeciwko Covid. W jakim stopniu możemy oczekiwać niezależnych decyzji, które są neutralne dla końcowych odbiorców?
Roczny budżet EMA na 2022 r. jest w dużej mierze finansowany z opłat farmaceutycznych
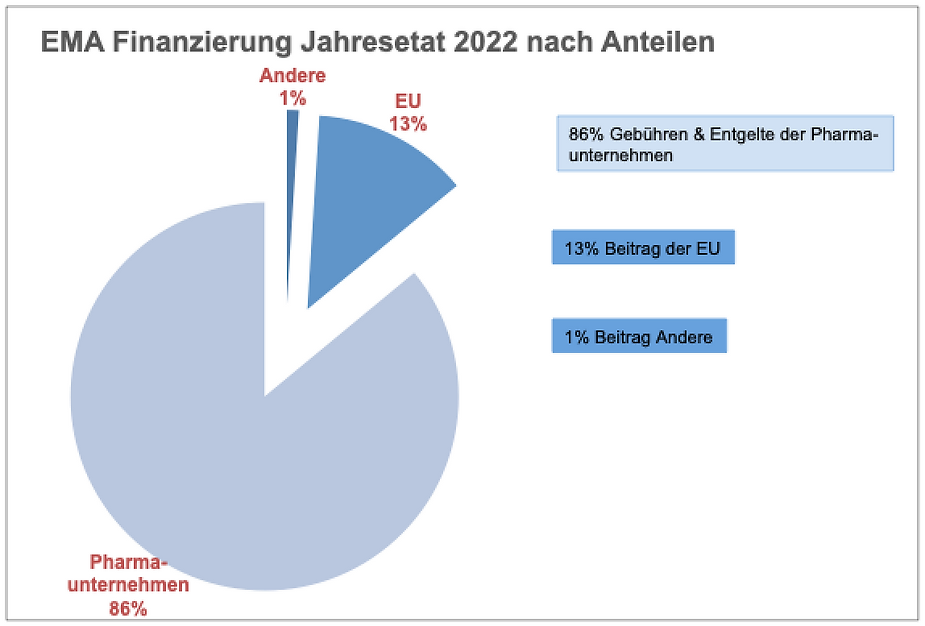
Finansowanie poprzez opłaty i prowizje
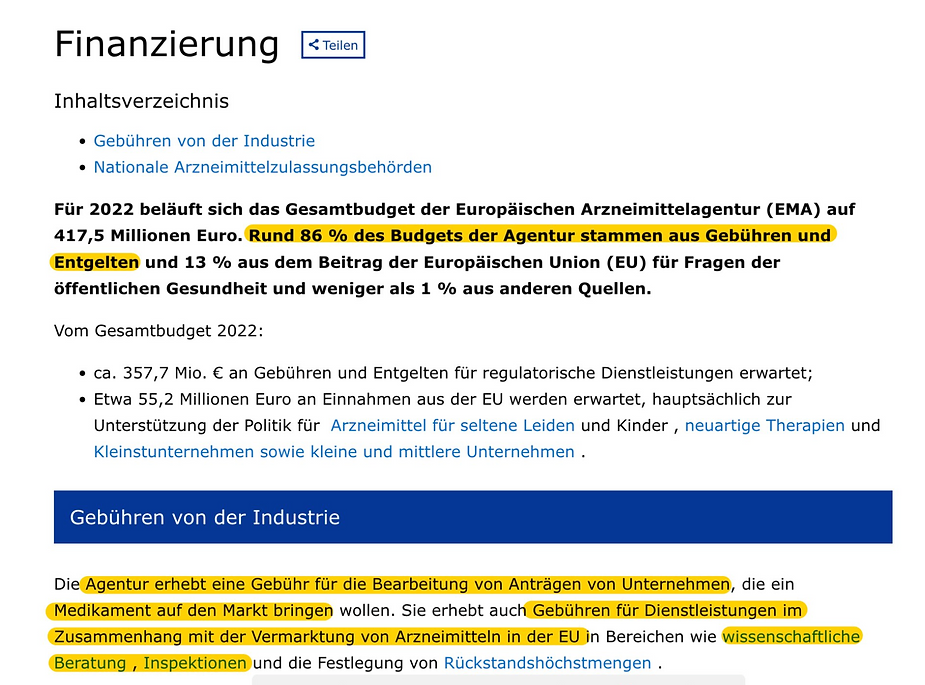
Według obecnego budżetu EMA 2022, 86% lub 358 z 417 milionów euro pochodzi bezpośrednio z opłat i należności przemysłu farmaceutycznego. Tylko 13% pochodzi z samej UE, tylko 1% z innych źródeł. EMA jest zatem finansowana głównie przez same firmy farmaceutyczne.
Dla porównania: w 2019 roku przed Coroną 294 z 340 milionów euro całkowitego budżetu pochodziło z przemysłu farmaceutycznego. W rezultacie firmy farmaceutyczne wniosły dodatkowe 64 miliony w 2022 r. w porównaniu z 2019 r.
„Agencja pobiera opłaty za wnioski o pozwolenie na dopuszczenie do obrotu , opłaty zmienności oraz opłaty roczne za zatwierdzone leki”.
„Nawet środki nadzoru nad bezpieczeństwem farmakoterapii przeprowadzane na szczeblu UE w odniesieniu do leków stosowanych u ludzi są finansowane z opłat wnoszonych przez posiadaczy pozwolenia na dopuszczenie do obrotu”.
Liczba wniosków o zatwierdzenie, wsparcie w fazie przed i po zatwierdzeniu oraz późniejszy monitoring po zatwierdzeniu, zależny od okresu użytkowania produktu, wpływają bezpośrednio i istotnie na wysokość rocznych obrotów EMA.
Konflikt interesów związany z modelem biznesowym
Powstaje teraz pytanie, w jakim stopniu ma to wpływ na liczbę zatwierdzeń. W jakim stopniu można z tego wywnioskować zależność między firmami farmaceutycznymi składającymi wniosek a EMA. Jedno jest pewne: im więcej leków zostanie dopuszczonych i wprowadzonych do obrotu, tym więcej opłat za kontrolę i monitoring farmaceutyczny uzależnione jest od okresu trwałości produktu. To oczywiście prowadzi do konfliktu interesów projektowych.
Ze względu na codzienną działalność i ścisłą współpracę między firmą farmaceutyczną a organem regulacyjnym istnieje również silne powiązanie z przemysłem farmaceutycznym pod względem czasu, w przeciwieństwie do powiązania z konsumentami końcowymi.
Emer Cooke, dyrektor EMA, był wcześniej szefem największej w Europie grupy lobbingowej dla przemysłu farmaceutycznego
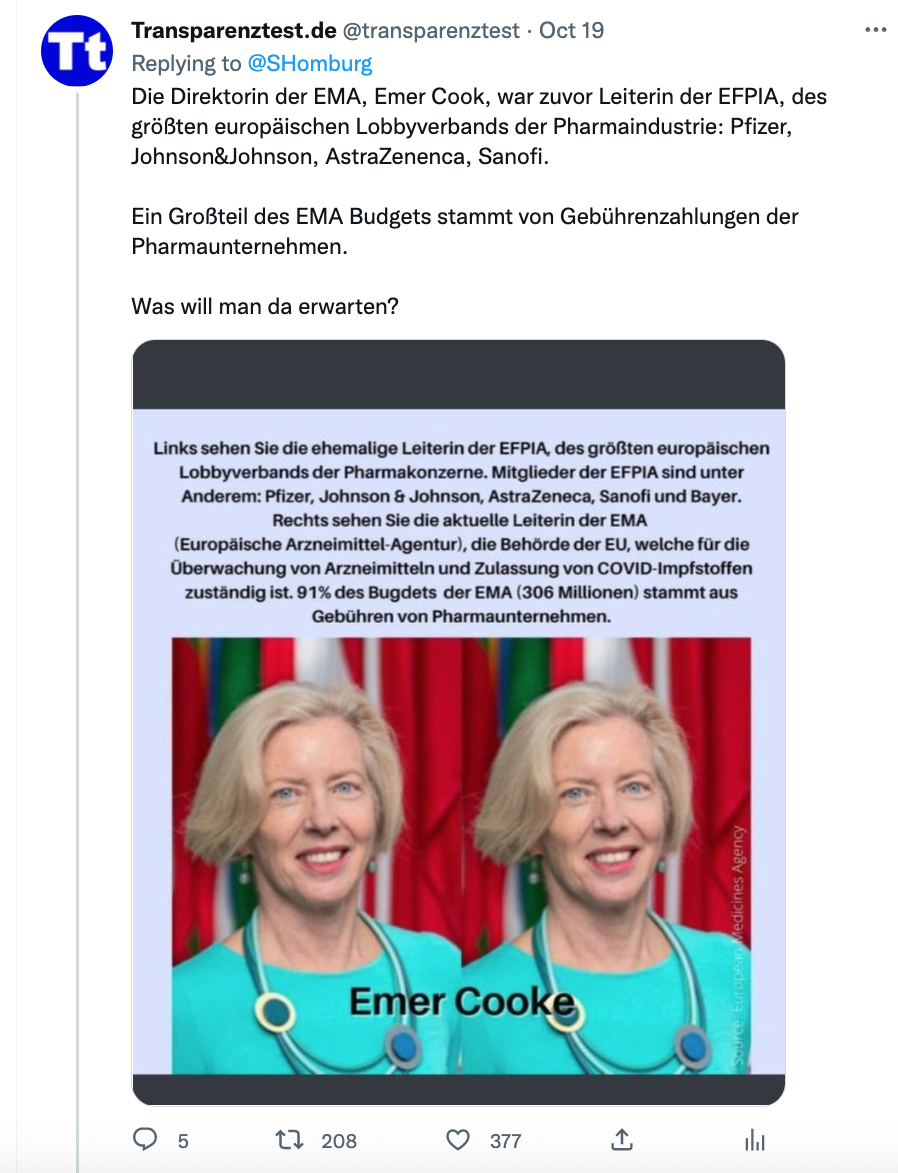
Organizacja medialna Politico potwierdza: „Pracowała też w europejskim lobby farmaceutycznym EFPIA”.
Niemiecki portal z wiadomościami biznesowymi pisze w tytule artykułu:
„Dyrektor UE ds. zatwierdzania szczepionek był lobbystą farmaceutycznym”.
Poniższy wpis na temat EFPIA można znaleźć w Lobbypedii:
„ Europejska Federacja Przemysłu i Stowarzyszeń Farmaceutycznych (EFPIA) to europejska organizacja patronacka przemysłu farmaceutycznego, której członkami jest 37 krajowych stowarzyszeń i 38 wiodących firm farmaceutycznych oraz 17 małych i średnich firm. Istnieje również stowarzyszenie zawodowe Vaccines Europe (VE) i 35 partnerów w dziedzinie badań. Wśród niemieckich członków jest Stowarzyszenie Producentów Leków Opartych na Badaniach (VfA).”
„EFPIA jest najważniejszą organizacją lobbingową w europejskim przemyśle farmaceutycznym z najwyższymi kosztami lobbingu, największą liczbą kontaktów z UE i kilkoma zaangażowanymi agencjami lobbingowymi. Jest także partnerem unijnych programów badawczych, takich jak Innovation Medicines Initiative (IMI), Największe partnerstwo publiczno-prywatne w Europie.”
Następujące firmy farmaceutyczne są wymienione na stronie internetowej EFPIA w dniu 19 października 2022 r.

Producenci szczepionek Covid Pfizer, Johnson & Johnson, Astrazeneca i Sanofi są członkami Europejskiej Federacji Przemysłu Farmaceutycznego EFPIA.
Według strony internetowej EMA, Emer Cooke pracowała dla EFPIA w latach 1992-1995 oraz w niepełnym wymiarze godzin w latach 1996-1998.
Przed objęciem obecnej roli była dyrektorem ds. działań regulacyjnych związanych z wyrobami medycznymi w WHO w Genewie od listopada 2016 r. do listopada 2020 r. Ta pozycja w WHO również nie jest wolna od wpływów farmaceutycznych. Ten wpływ ma tylko Fundacja Billa i Melindy Gates, która jest drugim największym darczyńcą WHO.
Emer Cooke jest odpowiedzialnym dyrektorem wykonawczym EMA od 16 listopada 2021 r. Ten moment zbiega się niemal równocześnie z rozpoczęciem kampanii szczepień przeciwko Covidowi.
Zadania EMA
EMA opisuje swoje zadania na swojej stronie internetowej w następujący sposób:
„Europejska Agencja Leków (EMA) jest zdecentralizowaną agencją Unii Europejskiej (UE) odpowiedzialną za naukową ocenę, nadzór i monitorowanie bezpieczeństwa leków w UE”.
„EMA została utworzona w 1995 r. w celu harmonizacji pracy istniejących krajowych organów regulacyjnych ds. leków . Wraz z utworzeniem w 2012 r. Komitetu ds. Nadzoru nad Bezpieczeństwem Farmakoterapii i Ryzyka (PRAC) EMA zaczęła odgrywać jeszcze ważniejszą rolę w nadzorowaniu bezpieczeństwa leków na całym świecie. w Europie.”
Opłaty i należności są należne za „żywotność” produktów wprowadzanych do obrotu w obszarach „oceny naukowej”, „doradztwa”, „wsparcia przed i po zatwierdzeniu”, „monitorowania”, „nadzór nad bezpieczeństwem farmakoterapii” i „oceny ryzyka” .
Im więcej produktów, tym więcej opłat jest pobieranych w całym łańcuchu monitorowania.
Podsumowanie testu przejrzystości
Wraz z zaskakująco szybkim zatwierdzeniem szczepionki Covid dla niemowląt od 6 miesiąca życia, EMA obniżyła ostatni próg zahamowania.
Szybkie zatwierdzenie z nielicznymi i wątpliwymi danymi
Zatwierdzenie nadeszło zaskakująco szybko i opierało się na niewielkiej ilości danych. Ponadto dane dotyczą jedynie oznaczania miana przeciwciał i nie dostarczają żadnych informacji o ich znaczeniu klinicznym. Po raz kolejny krytycznie obniżono standardy zatwierdzania. Nie przeprowadzono klinicznych randomizowanych badań zatwierdzających z udziałem niemowląt/dzieci, które wykraczałyby poza rejestrację wartości laboratoryjnych w postaci mian przeciwciał i dlatego nie mogły być brane pod uwagę.
To ponownie rodzi fundamentalne pytania dotyczące niezależności procesu decyzyjnego EMA.
Konflikt interesów związany z modelem biznesowym
Opłaty za wnioski o zatwierdzenie, opłaty za wsparcie w fazie przed i po zatwierdzeniu oraz opłaty za późniejszy bieżący monitoring produktu po zatwierdzeniu wpływają bezpośrednio i istotnie na roczne obroty EMA.
Stwarza to konflikt interesów związany z systemem: im więcej leków zostanie zatwierdzonych i wprowadzonych do obrotu, tym większe opłaty, zwłaszcza za kontrolę i monitorowanie leków przez całe życie. W języku ojczystym jest powiedziane
„Nie gryziesz ręki, która cię karmi”.
Zastąpienie długoletniego lobbysty farmaceutycznego na czele EMA – w sam raz na zatwierdzenie i rozpoczęcie szczepień – jest podejrzane i wyjątkowo niefortunne.
Wobec tych oczywistych finansowych i osobistych zależności EMA, brak reakcji ze strony EMA (brak publikacji wyników analiz sygnałów ostrzegawczych) ze względu na – bezwzględnie i względnie – nieproporcjonalnie wysoką liczbę zgłoszonych skutków ubocznych szczepień przeciw Covid może również być zrozumianym.
2 036 307 zgłoszonych osobistych zgłoszeń skutków ubocznych ADR szczepionek Covid w okresie około 20 miesięcy już stanowi ponad 110 % z 1821 211 zgłoszeń skutków ubocznych ADR wszystkich 5042 substancji zawartych w lekach / szczepionkach wymienionych w 2020 roku .
Duże systemy monitorowania, takie jak WHO VigiAccess, EMA EudraVigilance lub US VAERS nadal działają w połowie procesu raportowania. Jednak liczby prawdopodobnie nie będą kompletne.
Najpóźniej w momencie przetwarzania zgłoszeń ADR wydaje się, że nie jest to prawidłowe. Oczywiście nic się nie dzieje. Oczywiście sygnały ostrzegawcze są ignorowane. W tym celu kolejne szczepionki Covid są zatwierdzane i wprowadzane na rynek bez prawie żadnych zrozumiałych i wystarczających danych klinicznych.




